Energie en faseovergangen
Faseovergangen vinden plaats wanneer energie wordt toegevoegd of verwijderd uit een stof, waardoor de deeltjes anders bewegen of zich anders rangschikken. Dit leidt tot een verandering van de aggregatietoestand.
Hoe beïnvloedt energie faseovergangen?
Energie toevoegen
Als er energie wordt toegevoegd, gaan de deeltjes sneller bewegen en kunnen ze hun onderlinge krachten doorbreken. Voorbeelden:
- Smelten: Vast → vloeibaar, zoals ijs dat smelt tot water.
- Verdampen: Vloeibaar → gas, zoals water dat kookt en stoom wordt.
Energie verwijderen
Als er energie wordt onttrokken, bewegen de deeltjes langzamer en komen dichter bij elkaar. Voorbeelden:
- Bevriezen: Vloeibaar → vast, zoals water dat ijs wordt.
- Condenseren: Gas → vloeibaar, zoals waterdamp die dauw vormt.
Latente warmte
Latente warmte is de energie die wordt opgenomen of afgegeven tijdens een faseovergang, zonder dat de temperatuur verandert. Voorbeelden:
- Smeltwarmte: Energie nodig om een vaste stof vloeibaar te maken.
- Verdampingswarmte: Energie nodig om een vloeistof in gas om te zetten.
Het verwarmingsdiagram van water
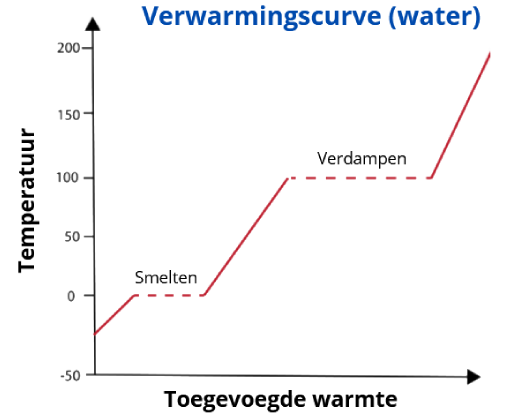
Het verwarmingsdiagram van water laat zien hoe water verandert van fase bij het toevoegen van warmte-energie:
- Segment 1: IJs warmt op tot 0°C.
- Segment 2: IJs smelt tot water bij constante temperatuur (0°C).
- Segment 3: Water warmt op tot 100°C.
- Segment 4: Water kookt en wordt stoom bij 100°C, terwijl energie wordt opgenomen.
Toepassingen van faseovergangen
Kennis van energie en faseovergangen wordt toegepast in veel gebieden:
- Koelkasten: Maken gebruik van verdampingswarmte om te koelen.
- Energieopslag: Faseovergangsmaterialen worden gebruikt in warmtebatterijen.
- Weervoorspelling: Verdampt en condenseert water in de waterkringloop.